El cáncer afecta a millones de personas en todo el mundo, es responsable del 23 por ciento del total de las muertes y constituye la segunda causa de fallecimientos, después de las enfermedades cardiovasculares
Un grupo interdisciplinario de investigadores de la Universidad Nacional de Río Cuarto está abocado a desarrollar la técnica que se denomina Terapia Fotodinámica.
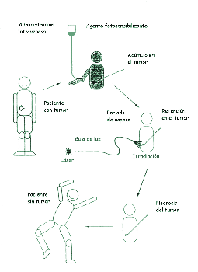
El trabajo apunta a conseguir nuevas drogas derivadas de porfirinas para el tratamiento de enfermedades neoplásticas, mediante terapia fotodinámica, que es un método alternativo para el tratamiento de tumores malignos, que involucra la administración de un fotosensibilizador, seguida por su activación por medio de la luz visible. Es un agente terapéutico que tiene la particularidad de ser retenido selectivamente por las células tumorales.
Un cuerpo normal y sano está formado por 30 billones de células, que viven en un condominio complejo e interdependiente en el que unas regulan la proliferación de otras. En condiciones normales, las células sólo se reproducen cuando reciben las instrucciones apropiadas que les envían otras células vecinas. De esta manera, cada tejido mantiene el tamaño y la forma adecuada a las necesidades del cuerpo.
Por el contrario, las células cancerosas transgreden este esquema, ignoran los controles normales de proliferación y siguen sus propias instrucciones internas de reproducción, a lo que se agrega que pueden emigrar del sitio donde se producen, invadir otros tejidos y formar masas en lugares distantes del cuerpo, lo cual es conocido como metástasis.
Con el tiempo, los tumores formados por esas células malignas se vuelven cada vez más agresivos y se tornan letales en cuanto empiezan a destrozar tejidos y órganos vitales.
Viviana Rivarola, licenciada en Microbiología y doctora en Ciencias Biológicas, está al frente de un equipo que viene llevando adelante este trabajo de investigación en la Universidad Nacional de Río Cuarto, el cual tiene como peldaño a alcanzar la selección de la molécula apropiada para estudios de terapia fotodinámica in vivo en un modelo de tumor animal.
La docente investigadora de la cátedra de Orientación Química Biológica de la UNRC comenta que la iniciativa tiene distintos aspectos, uno químico, otro biológico y otro fisiológico, al tiempo que agrega que este proyecto consiste en el diseño y la síntesis de quimioterapéuticos, que tienen la particularidad de ser sustancias que se pueden aplicar a las células y ser utilizadas en el futuro para tratamientos anticancerígenos, haciendo uso de la luz en combinación con ese tipo de agentes.
En este emprendimiento interdisciplinario trabajan profesionales de química, biología y de fisiología. Rivarola, en referencia a la marcha del trabajo de laboratorio, dice que hace poco que hemos iniciado el estudio de prueba. Algunas de estas moléculas primero se prueban en cultivos de células y luego en ratones, pues no todas cumplen con los requisitos necesarios para ser utilizadas en animales y agrega que en estos experimentos se contemplan, entre otras variables la toxicidad de los compuestos, en la oscuridad y en presencia de luz.
En cuanto al cáncer, la investigadora explica que es una enfermedad que empieza cuando una célula escapa de los mecanismos normales de división celular. Una célula normalmente tiene señales que dicen que se puede dividir o no y existe cierta armonía en un organismo, entre la vida y la muerte de la célula. Eso ocurre a nivel molecular. El material genético sufre cambios irreversibles, hace que los frenos en la división celular no se lleven a cabo y la célula empiece a dividirse en forma descontrolada.
Terapia fotodinámica
La terapia fotodinámica
ha comenzado a utilizarse en muchos países. En Estados Unidos, por
ejemplo, en el año 99 cuatro mil pacientes fueron atendidos con
esta técnica. Los resultados varían con el tipo de cáncer,
los más positivos se obtuvieron en casos de cáncer de piel.
Principalmente, esta terapia
se utiliza en cáncer de esófago, de piel , de pulmón
y básicamente, consiste en una molécula que es un fotosensibilizador,
que se llama así porque se incorpora a la célula. Una vez
dentro de la célula, produce una alteración del oxígeno
molecular y adquiere una forma tóxica, que se llama oxígeno
singlete, el cual altera componentes de la membrana que produce la muerte.
En este sentido, Rivarola
comenta que todavía no se ha encontrado un fotosensibilizador que
penetre exclusivamente en la célula tumoral y agrega que se necesita
la combinación del fotosensibilizador, la luz y el oxígeno
que está en todas las células. Se debe tener al organismo
en la oscuridad e iluminar solamente el tumor, para lo cual se penetra
una cánula, con lo que el tratamiento resulta eficiente.
¿Qué características
tiene el fotosensibilizador?
El fotosensi-bilizador que
los investigadores deben sintetizar y después probar, tiene que
ser un compuesto puro, que penetre en la célula tumoral
con mayor frecuencia que en la célula normal y además no
debe ser tóxico en la oscuridad, es decir, que por sí solo
no debe causar muerte, sino solamente cuando las células son iluminadas.
Por este motivo, no todos los fotosensibilizadores que los investigadores
prueban en cultivos de células son aptos para terapias fotodinámicas.
La muerte de la célula
puede ocurrir por dos procesos, por necrosis o por apoptosis. La muerte
por necrosis es descontrolada, la célula recibe un estímulo
nocivo y se producen cambios que son irreversibles, hay entrada de agua
en la célula, la cual se hincha, sufre ruptura de la membrana,
liberación de todo su contenido y eso ocasiona inflamación
en el animal o el ser humano.
La muerte por apoptosis,
que es la que se persigue con este tratamiento, es más silenciosa,
en el sentido de que la célula se retrae, se encoge, no pierde nunca
el contenido celular, sino que las células se particionan, forman
lo que se llaman los cuerpos apoptóticos, los cuales son fagocitados
por células vecinas.
Experimentaciones
Actualmente, se está
en la fase de experimentación con animales. Los investigadores han
comenzado a estudiar aspectos fisiológicos, luego de que el año
pasado trabajaron en cultivos celulares con algunas moléculas y
seleccionaron una (CF3) para analizar la toxicidad dentro del animal. Recientemente
se ha conseguido formar tumores en ratones, para luego poder realizar estudios
con terapia fotodinámica.
La fase de experimentación
incluye varios pasos. Lo primero que se ha hecho es ver si la molécula
es o no tóxica en la oscuridad, lo cual ya está concluido
en el caso de CF3. Luego, se inyectaron células capaces de producir
el tumor en animales. Ahora lo que se pretende es inyectar el fotosensibilizador
o el agente quimioterapéutico y observar la distribución,
es decir, si va preferentemente al tumor o a otros órganos, si causa
algún daño y si cuando el tumor es iluminado se produce la
regresión que se busca.
El estudio
En la Universidad se trabaja
en cultivo de células y la parte de irradiación se hace con
un proyector que está dentro de una cámara oscura, que ilumina
el cultivo de células o el tumor del animal.
A esta altura, cabe preguntarse
qué son las porfirinas, para qué sirven; qué características
tienen las drogas derivadas de porfirinas, cómo actúan; cuáles
son las enfermedades neoplásicas; en qué consiste la terapia
fotodinámica y qué utilidad tiene.
En este sentido, la doctora
Rivarola explica que las porfirinas son moléculas insolubles en
agua, que en la estructura química tienen muchos anillos y poseen
una estructura plana, lo cual hace que se comporten de una manera particular.
Los investigadores apuntan
a aprovechar la capacidad de las porfirinas de penetrar en la célula
y hacer reaccionar con la luz visible, produciendo algunos efectos en ella.
La terapia fotodinámica
consiste en la aplicación de estas porfirinas a las células,
con la finalidad de que penetren en ellas y cuando se iluminan con luz
produzcan su muerte y que en la oscuridad no lo hagan.
Primero se realiza la síntesis,
es decir, la purificación de la porfirina y luego tiene lugar
un estudio a nivel celular en cultivo de células.
Este estudio consiste en
hacer crecer en forma de monocapa -una sola capa de células- con
un medio de cultivo adecuado y agregarle la porfirna; tenerlas en la oscuridad
y ver si muere la célula cosa que puede ocurrir porque algunas
son tóxicas de por sí en la oscuridad-.
Luego a las que no son nocivas
en la oscuridad, se las ilumina en distintos tiempos, con diferentes dosis,
para ver si mueren.
Con posterioridad, a las
porfirinas que causan muerte con la luz, se las estudia respecto de si
las células se mueren por necrosis o por apoptosis.
Una vez culminada la etapa
del estudio en cultivo de células, se pasa a la investigación
en los animales, que consiste en ver si la porfirina es tóxica en
el ratón.
En la oscuridad y en la
luz
Este equipo de investigación
de la UNRC estudia la citotoxicidad en la oscuridad y en la luz por medio
de métodos químicos y morfológicos.
Los químicos implican
agregar un reactivo, que solamente cambia de color con células que
están vivas, con lo que se determina el porcentaje de células
vivas y muertas después del tratamiento.
Los estudios morfológicos
consisten en observar por microscopía de campo claro o también
por microscopía de fluorecencia y contar las células vivas
y las que están muertas, ya sea por necrosis o por apoptosis.
En este marco, lo que se
pretende es lograr tener el mayor porcentaje de células vivas en
la oscuridad y el mayor porcentaje de células muertas después
de 15 minutos de iluminación. En este marco, se ha logrado que solamente
el diez por ciento de células queden vivas, después de ese
cuarto de hora con luz.
El objetivo es seleccionar
las moléculas que pasan por todas estas etapas, que no sean tóxicas
en la oscuridad, que maten el mayor porcentaje de células con la
luz, que después no sean tóxicas en el animal y que cuando
se los ilumine, el tumor desaparezca.
Los investigadores
El equipo dirigido por Rivarola
tiene como codirector al Dr. Edgardo Durantini y cuenta con la participación
de los becarios de posgrado (CONICET): Mic. Maria Gabriela Alvarez, de
grado: Flavia Moran y Elisa Milanesio (Dir.: Dr. E. Durantini). Además
participan como
tesista de posgrado
Ines Yslas y como
alumna tesista de grado
Belen Rummie Vittar Los demás investigadores que participan son
Med. Vet. Mabel Bertuzzi, Dra. Gladys Mori y Dr. Jorge Bergesse.
Dra. Viviana Rivarola
Fac. de Ciencias Exactas / Dto. Biología Molecular
Tel: 0358 - 4676114 / EMail:vrivarola@exa.unrc.edu.ar
